 已关闭
已关闭
- 顶部Banner位
固定模块
设置

BPD
试用
AI
登录/注册
企业管理端
再次败给安慰剂!Brensocatib又一适应症临床失败
易享资讯
2026-04-10 14:50
近日,Insmed Incorporated公司公布了其在研药物Brensocatib用于治疗中重度化脓性汗腺炎(HS)的Ⅱb期临床试验(CEDAR研究)结果。数据显示,Brensocatib两个剂量治疗组在改善HS方面的表现均不及安慰剂组,试验的主要终点及所有次要终点均未达成。
这是继去年年底Brensocatib在慢性鼻窦炎(CRSwNP)适应症上临床失利后,该药物在炎症性疾病领域的又一次受挫。基于此项结果,Insmed已决定终止Brensocatib针对该适应症的后续开发。
再度未能超越安慰剂效应
CEDAR研究是一项随机、双盲、安慰剂对照的Ⅱb期试验,共纳入214名中重度HS成人患者,旨在评估每日一次10mg或40mg Brensocatib的疗效与安全性。
根据Insmed官方披露的数据,治疗第16周时,10mg组与40mg组患者的总脓肿和炎性结节计数较基线分别减少了45.5%和40.3%,而安慰剂组降幅为57.1%,疗效对比呈阴性。
安全性方面,Brensocatib组的不良事件发生率也相对较高。10mg治疗组有55.4%的患者报告了相关不良事件,高于安慰剂组的45.7%。此外,10mg组还报告了1例重度不良事件。
对于此次失败,Insmed方面解释称,HS领域缺乏成熟的动物模型,使得临床开发面临特殊挑战。本质上,这是一项概念验证性试验,既然未能达到预设目标,公司遂即做出终止开发的决定。
值得注意的是,去年12月Brensocatib在慢性鼻窦炎不伴鼻息肉(CRSsNP)的Ⅱb期研究(BiRCh)中,同样遭遇了类似的“安慰剂效应过强”的困境。当时数据显示,治疗24周后,10mg、40mg组患者的症状评分(sTSS)分别下降2.2分和2.33分,而安慰剂组下降了2.44分,未能显示出统计学差异。公司同样以缺乏动物模型为由,迅速终止了该适应症的开发。
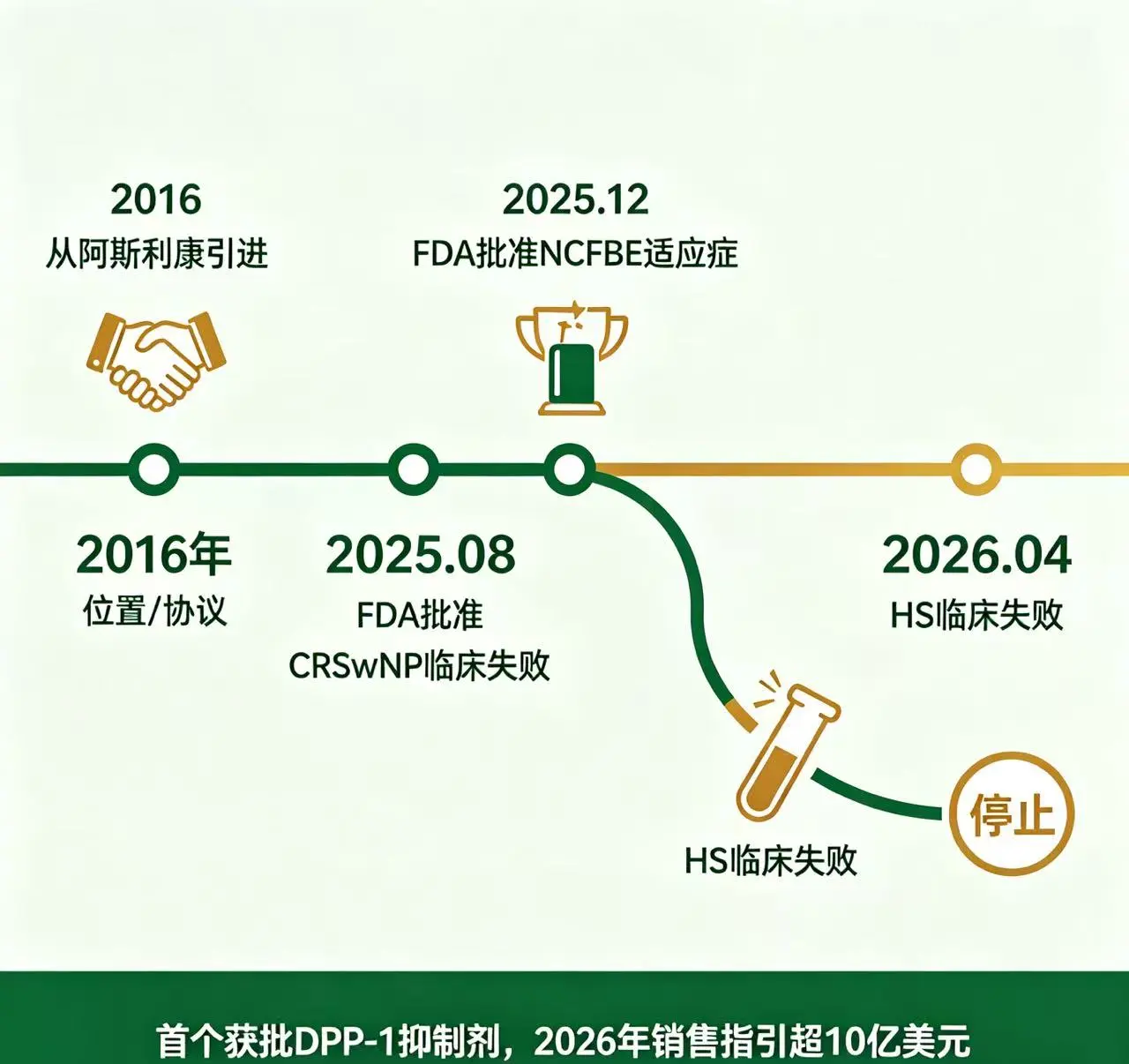
首个获批DPP-1抑制剂的商业前景
Brensocatib是一种口服二肽基肽酶1(DPP-1)抑制剂,为Insmed于2016年从阿斯利康引进,首付款3000万美元,后续里程碑款最高可达1.2亿美元。其作用机制在于通过抑制DPP-1/中性粒细胞丝氨酸蛋白酶轴,来减轻中性粒细胞介导的炎症反应。
尽管在皮肤与鼻窦炎症领域接连受挫,Brensocatib已在核心适应症上取得突破。2025年8月,该药物(商品名:Brinsupri)获美国FDA批准,用于治疗非囊性纤维化支气管扩张症(NCFBE),成为全球首款上市的DPP-1抑制剂,也是NCFBE领域的首个靶向治疗药物。
这一适应症的获批使其商业前景备受看好。Guggenheim分析师预测,仅凭NCFBE单一适应症,Brinsupri的销售峰值潜力便可达90亿美元。上市后,Brinsupri的市场表现也确实超出了预期——2025年全年销售额达1.727亿美元。在2025年财报中,Insmed对2026年Brinsupri的销售收入指引为不低于10亿美元。
在管线布局方面,Insmed并未止步于Brensocatib。公司正在推进下一代DPP-1抑制剂INS1033的开发,拟用于类风湿关节炎(RA)和炎症性肠病(IBD)的治疗,预计将于2026年提交IND申请。
参考来源:
1. Insmed官网新闻稿
2. Insmed 2025年第四季度及全年财报

返回顶部


