 已关闭
已关闭
- 顶部Banner位
固定模块
设置

周年庆试用
登录/注册
企业管理端
🧪蛋白浓缩又"漏"了?选对超滤管,告别低回收率!
易享实验
2026-04-01 18:06
在蛋白纯化、抗体药物研发、外泌体分离等实验中,超滤管几乎是每个分子生物学和生物化学实验室的“标配”。
但你是否遇到过:浓缩效率低、样品回收率差、膜与目标分子不兼容、甚至离心过程中漏液或破裂?或许这些问题的根源,不在于操作,而在于你选的那支超滤管。

超滤管本质不是“筛”是“压力驱动”
超滤本质上是以离心力为驱动力的膜分离过程。离心力迫使溶剂和小分子溶质通过半透膜,而大于截留分子量的分子被截留在浓缩管中。这一过程无需添加化学试剂,仅通过物理分离即可实现高纯度样品的制备。
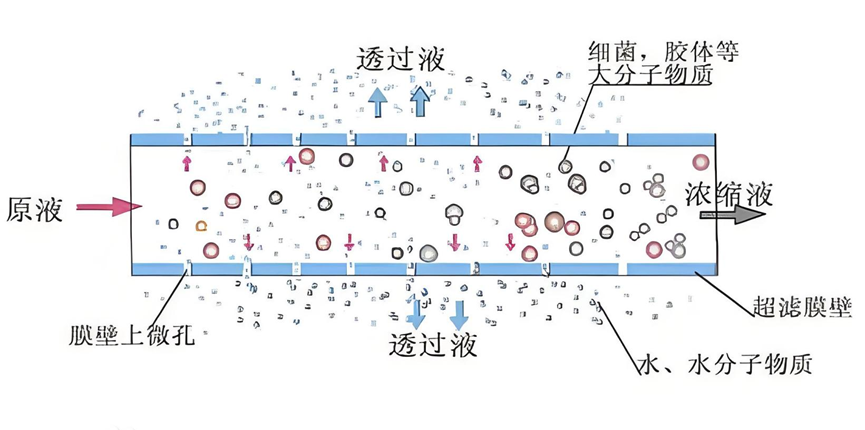
1. 截留分子量
截留分子量≠精准分子量切割,它通常定义为被膜截留90%以上的球状蛋白分子量。对于线性蛋白、核酸或其他构象分子,实际截留行为可能显著偏移。因此选型时,推荐选择截留分子量不应大于目标蛋白分子量的1/3。
2. 膜材质
再生纤维素(RC):亲水性强,非特异性吸附极低,回收率高,适合低浓度蛋白或珍贵样品。
聚醚砜(PES):通量高,耐pH范围宽,化学稳定性好,适合大多数蛋白质、核酸样品,是实验室通用型材质。
聚偏氟乙烯(PVDF):耐有机溶剂,适合高压操作,常用于病毒颗粒或外泌体的纯化。
3. 体积选择
样品初始体积应在超滤管标注有效体积的80%以内,避免离心平衡前即溢流。
4. 离心力耐受性与转子兼容性
不同超滤管最大耐受离心力差异显著,离心力过低会降低浓缩速度,过高则可能破坏膜或导致样品泄漏。可根据不同型号超滤管选择适合的离心机转子适配型号(固定角转子vs水平转子)。
实操:如何提高浓缩回收率?
预处理:新购的超滤离心管的有的超滤膜含有微量甘油,使用前可用Mili-Q水或缓冲液浸泡并置于冰箱预冷10分钟。之后倒出水,再将超滤管置于冰上预冷2-5分钟。如果干扰仍然存在,可用0.1M NaOH清洗,再用Mili-Q水清洗并甩干。
加样:移液枪移取适量样本加入超滤管中(操作时要轻,枪头不要刮破滤膜)。在加入样品时,需注意不得超过超滤管滤芯的最大体积。
平衡与离心:确保配对的超滤管质量与重心平衡,且滤芯的放置位置和方向必须一致,以确保各平行样品浓缩倍数的一致性,随后进行离心。
样本收集:离心后,大分子留在上层,小分子和溶剂通过膜进入下层。外管滤液为小分子物质和溶剂;内管液体为大分子物质,如需收集大分子物质,则另取外管,内管倒置1000×g离心1-2分钟。
处理与保存:若超滤管需重复使用,使用完的超滤管用纯水反复清洗5次,再用0.1M NaOH浸泡1-2小时,随后用75% 乙醇清洗,并用超纯水或缓冲液清洗3次。一般不建议重复使用超滤管超过5次。
易享是专注于生物产业的供采对接平台,“找产品”是平台的核心功能之一,目前汇聚了1700+ 上游商家,500W+ 产品,300+ 技术服务企业、15w+ 生物医药行业用户。
您可以在“找产品”搜索超滤管,即可找到目标产品和背后的供应商。每件产品均关联真实供应商,点击询价即可发起沟通,从询单到下单,链路清晰透明,帮助您在批量采购中精准锁定成本,告别反复询价、信息分散的烦恼。


返回顶部


