 已关闭
已关闭
- 顶部Banner位
固定模块
设置

周年庆试用
登录/注册
企业管理端
《2026 年 3 月全球生物医药前沿靶点进展月报:KAT6A/B、泛 KRAS、BTK 耐药等六大技术突破深度解析》
易享-研发职能社群资讯
2026-03-30 15:01
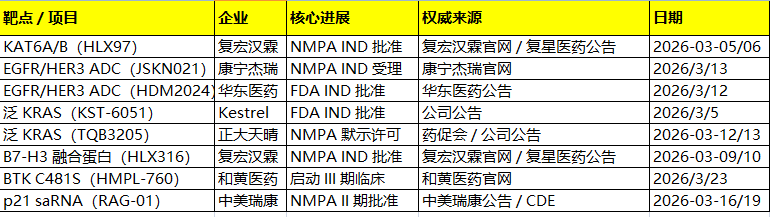
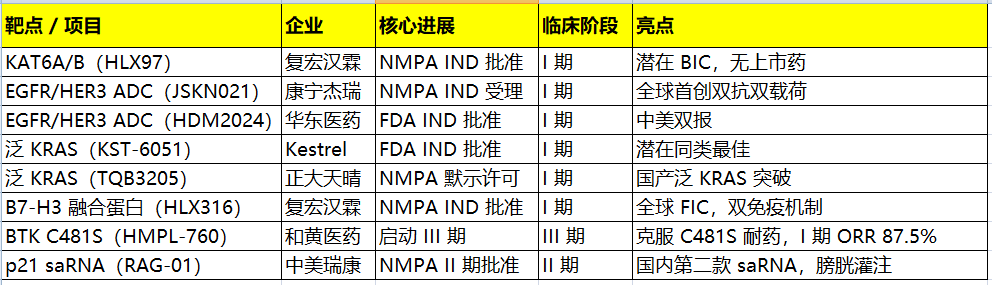
一、KAT6A/B 靶点(早期研发)
核心进展:复宏汉霖HLX97(口服小分子抑制剂)获 NMPA IND 批准,拟用于晚期 / 转移性实体瘤(含乳腺癌耐药)。
机制:抑制组蛋白乙酰转移酶 KAT6A/B,调控肿瘤增殖、分化与凋亡,克服内分泌治疗耐药。
临床阶段:I 期临床启动(2026-03-05)。
竞争格局:全球尚无上市药物;国内已有辉瑞、恒瑞、齐鲁、百济等 7 款进入临床,HLX97 为国产第 3 款。
亮点:潜在Best-in-class,高选择性、低血液毒性。
二、EGFR/HER3 双抗 ADC(临床前 / IND)
核心进展:2 个项目在 3 月取得里程碑,均为全球创新设计。
康宁杰瑞 JSKN021
类型:全球首创双抗双载荷 ADC(拓扑异构酶 I 抑制剂 + MMAE)。
进展:NMPA IND 受理,即将开展I 期(晚期实体瘤)。
临床前:CDX 模型中抑瘤效果显著优于单载荷 ADC。
类型:EGFR/HER3 双抗 ADC。
进展:FDA IND 批准(2026-03-10),国内同步申报。
赛道热度:百利天恒 Izalontamab brengitecan(IZA-BREN)在 NSCLC 中 ORR 近 70%,III 期推进中。
三、泛 KRAS 突变小分子抑制剂(I 期)
核心进展:国内外 2 款泛 KRAS 抑制剂获批临床,突破 G12C 单一突变局限。
Kestrel KST-6051
进展:FDA IND 批准(2026-03-05),启动 I 期剂量递增。
定位:潜在同类最佳,覆盖 G12C/D/V 等主流突变。
进展:NMPA 默示许可(2026-03-12),拟用于晚期恶性肿瘤。
机制:抑制 SOS1 介导的 KRAS 核苷酸交换,阻断下游通路。
格局:全球 10 + 款在研,多数处于 I 期;英矽智能等用 AI / 量子计算加速筛选。
B7-H3 唾液酸酶融合蛋白(实体瘤)
核心进展:复宏汉霖HLX316(B7-H3× 唾液酸酶融合蛋白)获 NMPA IND 批准,全球首创(FIC)。
机制:双功能破免疫逃逸 —— 阻断 B7-H3 抑制 + 去除肿瘤唾液酸化,恢复抗肿瘤免疫。
临床阶段:I 期(晚期 / 转移性实体瘤)。
临床前:体外及人源化小鼠模型显示强效抑瘤作用。
赛道:B7-H3 为热门免疫检查点,GSK 的 Risvutatugrezetecan 获日本孤儿药资格(2026-03-27)
五、BTK C481S 突变可逆抑制剂(临床)
核心进展:和黄医药HMPL-760(第三代非共价 / 可逆 BTK 抑制剂)启动III 期注册临床(DLBCL)。
机制:不依赖 C481 位点,同时抑制野生型与C481S 突变型BTK,克服耐药。
临床阶段:III 期(联合 R‑GemOx,复发 / 难治性 DLBCL),首患者给药(2026-03-20)。
关键数据:I 期 ORR 73.1%;经 BTK 抑制剂治疗患者亚组 ORR 达87.5%。
格局:礼来 Pirtobrutinib 已上市;默沙东 Nemtabrutinib 进入关键临床。
六、p21 saRNA(膀胱癌,靶点激活)
核心进展:中美瑞康RAG-01(靶向 p21 的 saRNA)获 NMPA 批准开展II 期临床(非肌层浸润性膀胱癌,NMIBC)。
机制:激活抑癌基因 p21,恢复 p53-p21 通路,抑制膀胱癌细胞增殖。
临床阶段:II 期(NMIBC),国内第二款获批临床的 saRNA 疗法。
支撑数据:澳洲 I 期显示 p21 显著上调、安全性良好、有完全缓解(CR)信号。
给药:膀胱灌注,LiCO™递送系统,局部高浓度、全身暴露低(<0.5%)。
免责声明:
1. 信息准确性说明:本内容已尽力追溯权威来源并核实核心信息,但不保证所有信息完全无遗漏、无更新偏差,相关研发进展(如临床阶段、数据指标)可能随时间推移发生变化,请以官方最新公告及监管机构公示为准。
2. 用途限制:本内容仅供易享咨询平台用户学习、交流、参考使用,不得用于商业推广、临床决策、投资研判等其他用途,严禁擅自篡改、转载、引用本内容用于非法用途。
3. 风险提示:生物医药研发具有高风险性、不确定性相关临床进展、疗效数据仅为阶段性结果,不代表最终上市获批及临床应用效果,任何基于本内容做出的决策,相关风险由决策方自行承担。
4. 版权与来源说明:本内容所引用的新闻稿、公告、数据等资料,版权归原发布方所有,本页面仅做合理引用与整理,若涉及版权侵权,请联系相关负责人删除。

返回顶部


